شبیه سازی شیمی کامسول برای استخراج نتایج در یک مدل الکتروشیمیایی. باتری لیمو در این پست وبلاگ ، ما در مورد روند کلی نحوه تنظیم معادلات الکتروشیمی و مدل های باتری از ابتدا صحبت می کنیم. هدف ما ، ایجاد یک باتری لیمو به عنوان باتری الکتروشیمی است.
آزمایش پروژه های کامسول
انجام پروژه کامسول یک تمرین آزمایشگاهی کلاسیک در شیمی مدرسه ، باتری لیمو است. با استفاده از یک لیمو ، یک قطعه مس (یک سکه یا برخی از سیم های مسی) و یک قطعه از جنس روی (مانند میخ گالوانیزه) ، می توان باتری ساخت که می تواند یک دستگاه الکتریکی کوچک را در یک ماده تغذیه کند.
شبیه سازی باتری الکتروشیمی و انجام شبیه سازی باتری الکتروشیمی با کامسول برای این مثال ، ما به این سوال خواهیم پرداخت، چه چیزی باعث می شود که باتری لیمو در طول زمان انرژی تولید کند و چگونه می توان جریان الکتریکی آن را بهبود بخشید؟
انجام پروژه کامسول در بهینه سازی توان خروجی مستقیماً به ولتاژ و جریان موجود در پایانه های الکترود مربوط می شود. این بدان معناست که مدل ما باید منابع اصلی ولتاژ و افت ولتاژ را در باتری گنجانده و ارزیابی جریان به این معنی است که انتقال بار (یونها و الکترون ها) نیز باید به طریقی لحاظ شود.
برای بهبود توان چه اقداماتی را می توان انجام داد؟ در ابتدا دانستن این مسئله گاهی اوقات دشوار است ، اما با توجه به محدودیت های موجود در مواد (لیمو ، مس و روی) ، یک فرض احتمالی این است که تنها راه تقویت عملکرد با تغییر در پیکربندی هندسی (قرار دادن) الکترودها خواهد بود.
در نتیجه ما باید یک مدل وابسته به زمان و معادلات دیفرانسیلی وابسته به مکان تعریف کنیم. تمام معادلات استفاده شده دراین ماژول شرایط مرزی مذکور را دارد و برای شبیه سازی باتری الکتروشیمی کفایت می کند.
انجام پروژه کامسول و واکنش های شیمیایی مربوط به باتری
حال ، در مورد اینکه چه نوع مواد شیمیایی و واکنش هایی را باید در مدل خود بگنجانیم.
با بررسی از اطلاعات تغذیه ای لیمو ، مشخص می شود که این الکترولیت از اسید سیتریک (300 میلی متر = 3/0 مول در لیتر) و اسید اسکوربیک (3 میلی متر) تشکیل شده است ، هر دو اسیدهای ضعیفی هستند که با pH تقریبی 2 بافر می شوند (که مربوط به غلظت پروتون 10 میلی متر) همچنین ترکیبی از یون های اضافی وجود دارد که برجسته ترین کاتیون ها پتاسیم (35 میلی متر) و کلسیم (7 میلی متر) هستند. همچنین مقداری کمیاب یون روی (9 میکرومولار) و مس (6 میکرومولار) قبل از معرفی الکترودهای ما در لیمو وجود دارد. علاوه بر این ، یک دسته آنیون (مانند کلراید) وجود دارد که با کاتیون ها مطابقت دارد ، زیرا قسمت عمده ای از الکترولیت ها همیشه خنثی هستند.
با توجه به اینکه این دو الکترود به ترتیب از فلزات Cu و Zn تشکیل شده اند و ممکن است این مواد حل شوند ، واکنش های الکترود زیر منطقی به نظر می رسد که برای تجزیه و تحلیل بیشتر در نظر گرفته شود.

در ادامه ، پتانسیل های تعادل بر حسب واحد si مشخص میشود:
برای غلظت های مشخص شده از اطلاعات متریال بالا استفاده می کنیم. ما با استفاده از معادله Nernst محاسبات مربوطه را انجام می دهیم. همچنین در این مرحله از فلش های دو جهته برای همه واکنشها استفاده می کنیم که نشان می دهد واکنشها کاملاً برگشت پذیر هستند و ممکن است در هر جهتی پیش روند.

از آنجا که الکترولیت آبی است ، یون های پروتون و هیدروکسید وجود دارد که به دلیل وجود اتوپروتولیز آب در سراسر تفاله لیمو به طور همگن وجود دارد.
با این حال ، به دلیل pH اسیدی ، غلظت هیدروکسید را ناچیزدر نظر می گیریم.
در سیستم های آبی ممکن است هیدروکسیدهای فلزی تشکیل شود. با این حال ، با مراجعه به نمودارهای Pourbaix برای Zn و Cu مشخص می شود که برای pH کم ، به احتمال زیاد در لیمو تشکیل نمی شوند.
آبی بودن الکترولیت نیز به این معنی است که بسته به پتانسیل الکترود ، اکسیژن و هیدروژن ممکن است در الکترودها تشکیل شده و یا مصرف شوند.
این دو واکنش ممکن است روی هر دو الکترود رخ دهد ، اگرچه در اینجا ما به طور کلی سرعت حرکت سریعتر روی الکترود مس را فرض می کنیم.
پتاسیم و کلسیم موجود در اطلاعات متریال دارای پتانسیل های انحلال استاندارد پایین تر از روی و مس هستند ، و این بدان معنی است که تا حد زیادی روی هیچ الکترود رسوب نمی کنند. به همین ترتیب ، گاز کلر دارای پتانسیل استانداردی بالاتر از اکسیژن است و بنابراین باید ولتاژ مربوط به آنرا ناچیز در نظر بگیریم.
انجام پروژه کامسول شرایط مرزهای سیستم و انتخاب هندسه
وقتی نوبت به قطعات روی و مس می رسد ، رسانایی این فلزات در مقایسه با تفاله لیمو بسیار زیاد است ، بنابراین مدل سازی پتانسیل الکتریکی فلزات به عنوان شرایط مرزی کافی است. در نتیجه این ، و بحث فوق ، مدل باتری پیشنهادی کاملاً تحت تأثیر آنچه در الکترولیت (تفاله لیمو) می گذرد و واکنش های موجود در سطوح الکترود ، انجام می شود. از این رو سطح خارجی لیمو را به استثنای الکترودهای فلزی به عنوان مرزهای سیستم انتخاب می کنیم.
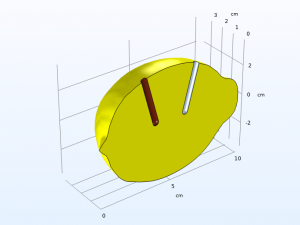
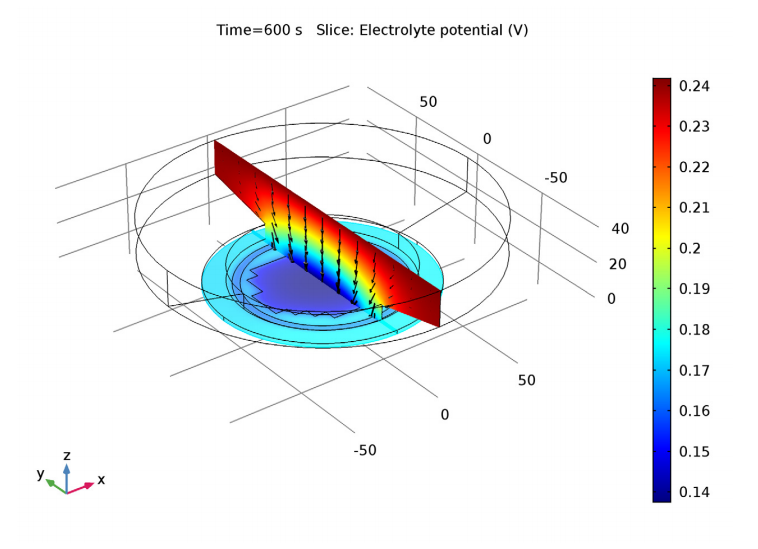
همچنین ، هنگام ساخت هندسه مدل ، تقارن را با برش دادن نصف لیمو برای صرفه جویی در منابع محاسباتی در نظر می گیریم. یعنی محیط شبیه سازی 2 بعدی متقارن است.
در نتایج نشان داده شده در زیر ، ما برای مدل سازی باتری لیمو از رابط توزیع جریان سوم ، از الکترولیت در آموزش شبیه سازی انجام پروژه با نرم افزار کامسول استفاده می کنیم. انتقال بارها را با یک رسانایی ثابت ، انتقال بارها توسط معادلات Nernst-Planck ، واکنش های الکترود بر اساس قانون جرم ساخته شده در سینتیک Butler-Volmer و محاسبه مبتنی بر معادله Nernst از پتانسیل های تعادل را تعریف می کنیم.
انجام شبیه سازی کامسول و آموزش کامسول
در شبیه سازی ، چرخه بار استفاده شده که در 1 دقیقه از شرایط اولیه (مقادیر پارامترهای مربوط به متریال) ، و پس از آن 1 دقیقه بار در 0.5 میلی آمپر و 1 دقیقه شرایط بدون بار الکتریکی است.
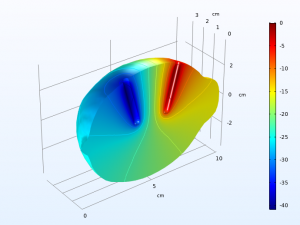
شکل زیر ولتاژ و جریان حاصل از شبیه سازی را نشان می دهد. در ابتدا ، هنگامی که الکترودها به لیمو وارد می شوند ، به نظر می رسد نوعی حالت استاتیک ایجاد می شود ، ولتاژ سلول به آرامی به 0.9 ولت افزایش می یابد. در t = 1 دقیقه ، یک افت ولتاژ قابل توجه از ولتاژ مدار باز به یک ولتاژ عملیاتی در حدود 0.1 ولت وجود دارد.
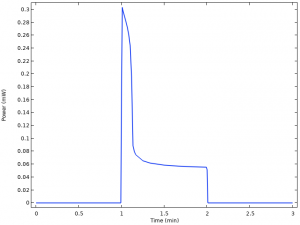
با ضرب ولتاژ سلول با جریان ، می توانیم خروجی سلول را نیز ترسیم کنیم. فقط چند ثانیه پس از قطع شدن مدار، بارالکتریکی ، از 0.3 تا 0.06 میلی وات کاهش می یابد.
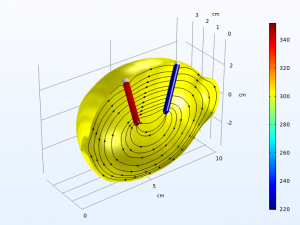
شبیه سازی و آموزش کامسول بهبود سینتیک الکترود ، که در الکترود Zn و برای مجموعه مقادیر پارامتر ما بیشترین تأثیر را در دو قطبی شدن سلول دارد ، دستیابی به آن بدون تغییر در الکترودها یا الکترولیت بسیار دشوار است. با این حال ، فعالیت کاتالیزوری نیز ممکن است با افزایش مقدار سطح موجود الکترود-الکترولیت بهبود یابد. دلیل این امر این است که تمام جریان باید از رابط های الکترود-الکترولیت روی هر الکترود عبور کند و افت ولتاژ مربوط به واکنش الکترود هرچه چگالی جریان بیشتر شود. با افزایش سطح موجود برای واکنش الکترود ، چگالی جریان محلی در هر منطقه الکترود کاهش می یابد و به نوبه خود افت ولتاژ مربوطه نیز کاهش می یابد.